
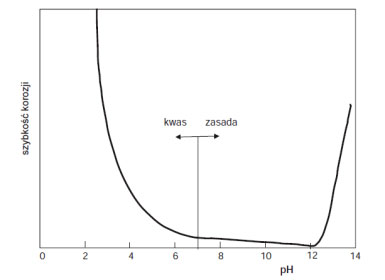
Rys. 2. Zależność szybkości korozji powłoki cynkowej od odczynu występującego w środowisku korozyjnym [na podstawie 3]
Kolejnym czynnikiem wpływającym na trwałość powłoki cynkowej jest agresywność środowiska korozyjnego. Norma PN-EN ISO 14713-1 określa ogólną klasyfikację środowiska korozyjnego i podaje grubość powłoki cynkowej, która powinna być zastosowana w danych warunkach agresywności atmosfery [4]. Nie uwzględnia przy tym różnorodności budowy morfologicznej powłoki cynkowej, a na różnych gatunkach stali jest ona bardzo zróżnicowana [5, 6]. W tab. 1 przedstawiono przewidywaną trwałość powłoki cynkowej w różnych środowiskach korozyjnych.
Mechanizm korozji atmosferycznej cynku jest różny w zależności od agresywności czynników korozyjnych oraz ich nasilenia w danym środowisku i w danym miejscu na powierzchni ocynkowanego wyrobu. Im bardziej agresywne warunki korozyjne, tym szybciej zachodzą reakcje i tym wyższa szybkość degradacji powłoki cynkowej. W przypadku występowania zanieczyszczeń atmosfery, np. związków siarki, chloru, w zmiennych warunkach wilgotności i temperatury, tworzą się produkty korozji cynku o dużej rozpuszczalności w wodzie, co powoduje zmniejszanie grubości warstwy ochronnej oraz jej porowatość. Najważniejszym czynnikiem wpływającym na intensywność korozji atmosferycznej jest czas zawilgocenia powierzchni elementu − wilgoć jest niezbędna do rozpuszczenia korozyjnych mediów z atmosfery (tlenków siarki, chlorków, tlenków azotu). Determinuje ona przebieg reakcji elektrochemicznych na powierzchni powłoki cynkowej [7].
Przebieg korozji powłoki cynkowej od momentu jej wytworzenia
Proces korozji atmosferycznej powłoki cynkowej w większości przypadków ma charakter korozji ogólnej, a powierzchnia powłoki bezpośrednio po jej wytworzeniu na stali jest wysoce aktywna [1–3]. Cynk bardzo szybko reaguje z utleniaczami występującymi w atmosferze już na etapie magazynowania w cynkowni. Skład obecnych na powierzchni produktów korozji cynku zależy od stopnia agresywności środowiska, składu tego środowiska i wilgotności.
W suchych warunkach składowania, w pierwszej dobie ekspozycji na działanie atmosfery, produktem korozji cynku jest tlenek cynku ZnO, który nie ma właściwości ochronnych. Pokrywa on równomiernie całą powierzchnię cynku. Pod wpływem wilgoci zamienia się w hydroksytlenki cynku – mieszaninę ZnO oraz Zn(OH)₂. Ilość tych produktów jest nieznaczna bez dostępu wilgoci (pary wodnej), jednak podczas nawet krótkotrwałej ekspozycji na jej działanie zaczyna być zauważalna [7]. Z tego też powodu, szczególnie podczas deszczowej pogody oraz w obecności rosy, na powierzchni powłoki cynkowej może powstawać tzw. biała korozja. Jej obecność jest dopuszczalna zapisami normy PN-EN ISO 1461 [8], jednak niepożądana i bardzo nielubiana przez wytwórców konstrukcji stalowych ze względu na znaczne pogorszenie estetyki wyrobów ocynkowanych. Wygląd powłoki cynkowej z obecną na powierzchni „białą korozją” przedstawiono na rys. 4.
W bardziej agresywnych warunkach korozyjnych reakcje elektrochemiczne zachodzą, niestety, szybciej, a ich produkty nie stanowią równomiernej warstewki ochronnej. Wtedy na powierzchni powłoki cynkowej następuje dynamiczne tworzenie się i rozpuszczanie wyżej opisanych związków chemicznych. W wyniku oddziaływania atmosfery morskiej, jak to ma miejsce w przypadku prezentowanej korozji ramy przyczepy (rys. 1), ochronny hydrocynkit przekształca się w hydroksychlorek cynku Zn₅(OH)₈Cl₂ [1]. Przy zawartości w środowisku minimum 25 mg/cm² jonów chlorkowych następuje ich adsorpcja na powierzchni i przebudowa struktury warstwy przypowierzchniowej [9]. Chlorkowe produkty korozji cynku są przeważnie nierozpuszczalne i nie wymywają się z powierzchni cynku, ale – niestety – nie są zbyt estetyczne. Ubytek grubości powłoki cynkowej w środowisku morskim wynosi od 8 do 12 µm/rok [1].
W atmosferze przemysłowej zawierającej SO₂ tworzą się na powierzchni powłoki cynkowej siarczany i hydrosiarczany, które mają swój wkład w tworzenie się warstwy ochronnej. Większość z nich jest jednak rozpuszczalna w kwaśnym środowisku. Szybkość korozji cynku jest wtedy jeszcze wyższa niż w przypadku atmosfery morskiej.








