

Tab. 1. Trwałość ogniowej powłoki cynkowej w różnych środowiskach korozyjnych [na podstawie 4]
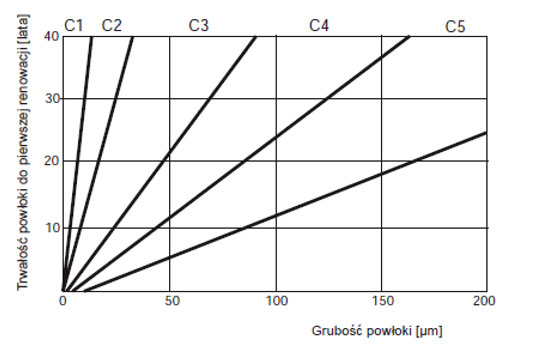
Rys. 3. Przewidywana trwałość powłoki cynkowej w zależności od warunków środowiska korozyjnego i grubości [na podstawie 4]
Jakie działania należy podjąć, aby zwiększyć trwałość zabezpieczenia korozyjnego?
Ze względu na powyżej opisane ograniczenia stosowania powłok cynkowych oraz mechanizm tworzenia się naturalnej warstwy pasywnej na powierzchni cynku warto zastanowić się już na etapie projektowania systemu ochronnego nad warunkami jego eksploatacji. Jeżeli wymagana jest wysoka estetyka powierzchni powłoki cynkowej oraz zachowanie połysku metalicznego w okresie składowania nawet podczas deszczowej aury i w efekcie niekorzystnej eksploatacji wyrobów, warto zastosować dodatkową obróbkę powierzchniową w postaci pasywacji polimerowej, chromianowej (oczywiście, z trójwartościowym chromem) czy fosforanowej. Widok powłoki cynkowej po pasywacji polimerowej na ramach przyczep przedstawiono na rys. 5. Widoczny jest pozytywny efekt wizualny, a wysoka estetyka pokrywanego wyrobu jest zachowana.
W warunkach eksploatacji systemu duplex, w przypadku przebicia powłoki malarskiej, funkcje zabezpieczenia antykorozyjnego przejmuje powłoka cynkowa. Ciągła warstwa cynku oraz warstwa faz międzymetalicznych Fe-Zn w powłoce cynkowej stanowi barierę oddzielającą stop żelaza od środowiska korozyjnego. W wyniku korozji elektrochemicznej tworzy się stabilna mieszanina tlenku, i węglanu cynku, których jednolita warstewka wypełnia szczeliny w powłoce malarskiej i w ten sposób chroni powierzchnię stali. Objętość związków cynku jest niewiele większa od cynku i faz żelazo−cynk, więc nie następuje odwarstwienie się lakieru od podłoża. Jak wspomniano wcześniej, w przypadku uszkodzenia samej powłoki, cynk jako metal o niższym potencjale elektrochemicznym od żelaza staje się anodą w ogniwie korozyjnym i ulega destrukcji, protektorując podłoże stalowe.
Jeżeli tylko pomalujemy konstrukcję stalową, to samodzielnie występująca powłoka malarska stanowi jedynie ciągłą barierę dla reakcji związków utleniających obecnych w środowisku korozyjnym z powierzchnią stali. Przerwanie ciągłości powłoki ochronnej będzie w tym przypadku skutkować powstawaniem ogniwa korozyjnego i natychmiastowym rozpoczęciem procesu korozji elektrochemicznej elementu. W wyniku utleniania i redukcji pomiędzy warstwą powłoki malarskiej a podłożem stali tworzą się uwodnione tlenki żelaza o większej objętości w porównaniu z samym żelazem: FeO−Fe₂O₃. Proces postępuje ze znaczną szybkością, prowadząc do tworzenia pęcherzy i odpadania powłoki malarskiej od podłoża cynkowego.













